课题组成员陈驰、张鹏飞等制备并报道了一种pH响应长衰减近红外掺杂型量子点,并将这种量子点用于基于荧光寿命的活体pH成像。这一工作近日被接受并发表于Chem Comm. (影响因子6.72),并被选为inside Cover。题目为“Long-Decay Near-Infrared-Emitting Doped-Quantum Dots for Lifetime-Based in Vivo pH Imaging. 2015, DOI: 10.1039/C5CC03046C.” Author(s): C. Chen, P.F. Zhang, L. Zhang, D.Y. Gao, G.H. Gao, Y. Yang, W.J. Li, P. Gong, and L.T. Cai*.
(原文链接 http://pubs.rsc.org/en/content/articlelanding/2015/cc/c5cc03046c)
Category Archives: 最新科研动态
最新科研动态
2015.04.14,李明星、刘朋等文章发表于ACS Appl. Mater. Interfaces!
课题组成员李明星、刘朋等成员通过将诱导凋亡的多肽纳米颗粒化,自身具有促进肿瘤细胞凋亡的功能,同时可用于载药,对靶向治疗肿瘤和增强化疗药物敏感性提供新的思路和方法。近日,相关成果已被ACS Appl. Mater. Interfaces接收发表(影响因子5.9),题目为”Smac Therapeutic Peptide Nanoparticles Inducing Apoptosis of Cancer Cells for Combination Chemotherapy with Doxorubicin” DOI: 10.1021/acsami.5b00329. Author(s): Mingxing Li, Peng Liu, Guanhui Gao, Jizhe Deng, Zhengyin Pan, Xu Wu, Gaofeng Xie, Caixia Yue, Chi Hin Cho, Yifan Ma, Lintao Cai*.
(原文链接 http://pubs.acs.org/doi/full/10.1021/acsami.5b00329)
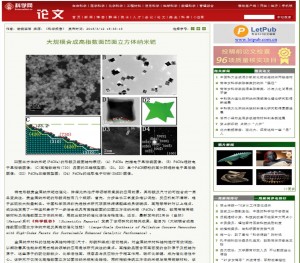
2015.03.12,科学网报道课题组最新成果:大规模合成高指数面凹面立方体纳米钯
2015.3.12,科学网报道了蔡林涛课题组谢晓滨、高冠慧等研究组成员的最新成果:大规模合成高指数面凹面立方体纳米钯,并具备高效催化活性与稳定性。这一工作近日被接受并发表于2月份《自然》(Nature)系刊Scientific Reports,题目为“Large-Scale Synthesis of Palladium Concave Nanocubes with High-Index Facets for Sustainable Enhanced Catalytic Performance” Author(s):Xiaobin Xie, Guanhui Gao, Zhengyin Pan, Tingjun Wang, Xiaoqing Meng, Lintao Cai*.
科学院刊登链接:http://paper.sciencenet.cn//htmlpaper/201531215331366935861.shtm
原文链接:http://www.nature.com/srep/2015/150217/srep08515/full/srep08515.html
2015.02.17,谢晓滨、高冠慧等文章发表于Scientific Reports!
特定形貌贵金属纳米钯在催化、生物标记、光谱学及肿瘤治疗等领域有重要的应用前景。其形貌及尺寸的可控合成一直备受关注,贵金属纳米钯的形貌调控有几个瓶颈:首先,分步生长工艺复杂难以调控;反应机制不清晰,难于实现放大批量制备。课题组成员谢晓滨、高冠慧等人针对以上难点,成功地发展了一种温和条件下一步法合成具有高指数面的立方凹面体纳米钯(PdCNs)颗粒,该研究不仅简化纳米钯制备路径,进一步提高其催化活性,较同等商用钯碳及低指数面立方体纳米钯,该纳米晶展现出较好的催化活性与稳定性,,该立方凹面体纳米钯表现出更加优越的高催化和长循环性能。近日,相关成果已被Nature系刊Scientific Reports接收发表(影响因子5.078),题目为”Large-Scale Synthesis of Palladium Concave Nanocubes with High-Index Facets for Sustainable Enhanced Catalytic Performance” doi:10.1038/srep08515. Author(s): Xiaobin Xie, Guanhui Gao, Zhengyin Pan, Tingjun Wang, Xiaoqing Meng, Lintao Cai*.
(原文链接 http://www.nature.com/srep/2015/150217/srep08515/full/srep08515.html)
2014.12.03,盛宗海、胡德红等文章发表于ACS Nano!
课题组成员盛宗海、胡德红等人通过程序化自组装制备了一种智能化的白蛋白吲哚菁绿诊疗一体化纳米颗粒,用于荧光/光声双模态成像引导的肿瘤协同光学治疗。这一工作近日被ACS Nano杂志接收,(影响因子12.033),题目为“Smart Human Serum Albumin-Indocyanine Green Nanoparticles Generated by Programmed Assembly for Dual-Modal Imaging-Guided Cancer Synergistic Phototherapy”Author(s): Zonghai Sheng, Dehong Hu, Mingbin Zheng, Pengfei Zhao, Huilong Liu, Duyang Gao, Ping Gong, Guanhui Gao, Pengfei Zhang, Yifan Ma, and Lintao Cai. DOI: 10.1021/nn5062386
2014.8.25,科学网报道课题组最新成果:二维近红外光学编码技术
2014.8.25,科学网报道了蔡林涛课题组陈驰、张鹏飞等研究组成员的最新成果:合成了一种具有超长寿命的近红外量子点,并利用其荧光寿命和波长,实现新的二维近红外光学编码。这一工作近日被接受并发表于 Advanced Materials(影响因子14.829),题目为“Near-Infrared-Emitting Two-Dimensional Codes Based on Lattice-Strained Core/(Doped) Shell Quantum Dots with Long Fluorescence Lifetime” Author(s): Chi Chen+, Pengfei Zhang+, Guanhui Gao, Duyang Gao, Yong Yang, Hong Liu, Yuhui Wang, Ping Gong, Lintao Cai*.
科学院刊登链接:http://paper.sciencenet.cn//htmlpaper/20148181481443834277.shtm
2014.8.4-2014.8.7,本课题组成员参加中国化学会第29届学术年会!
8月4日至7日,中国化学会第29届学术年会在北京大学召开。本届年会以“美丽化学”为主题,规模创历届年会之最,参 会代表达到8000余人,交流论文达 5180余篇,年会期间共安排896个分会邀请报告、1230个分会口头报告,3056个墙报展讲。课题组蔡林涛研究员及课题组成员赴京参加。期间,蔡林涛研究员及课题组成员盛宗海、张鹏飞等分别就课题组近年来在量子点等纳米材料的合成、肿瘤靶向纳米探针的构建、多模态成像及诊疗一体化、生物正交活病毒标记及活体示踪等方面的研究进展以口头报告的形式向参会学者进行了介绍,并与参会学者就纳米生物医学中的化学问题进行了深入探讨。课题组其他成员也通过论文海报的方式围绕纳米生物技术领域的前沿科学问题与其他研究者展开交流和讨论。
2014.07.01,陈驰、张鹏飞等文章接收发表于Advanced Materials!
课题组成员陈驰、张鹏飞等开发并合成了一种具有超长寿命的近红外量子点,并利用其荧光寿命和波长,实现新的二维近红外光学编码。这一工作近日被接受并发表于 Advanced Materials(影响因子14.829),题目为“Near-Infrared-Emitting Two-Dimensional Codes Based on Lattice-Strained Core/(Doped) Shell Quantum Dots with Long Fluorescence Lifetime” Author(s): Chi Chen+, Pengfei Zhang+, Guanhui Gao, Duyang Gao, Yong Yang, Hong Liu, Yuhui Wang, Ping Gong, Lintao Cai*
2014.06.26, 郑明彬、赵鹏飞等文章接收并发表于《科学通报》
由课题组内郑明彬、赵鹏飞等综述了量子点、纳米金/纳米银、碳纳米管/石墨烯、磁性纳米颗粒、脂类/聚合物类纳米颗粒等纳米颗粒的最新研究进展。该文章题目为“纳米技术在癌症诊疗一体化中的应用”被国内著名期刊《科学通讯》收录发表。
2014.06.19. 方胜涛等文章接收发表于Nanoscale
2014.06.19. 课题组成员方胜涛、吴蕾等首次利用多肽纳米胶束系统性传递ZEB1 siRNA用于肺癌治疗,结果显示该纳米系统能够抗肿瘤转移和增强肿瘤细胞对化疗药物的敏感性,为癌症的治疗提供了新的思路和策略。文章接收发表于Nanoscale(IF=6.233),题目为:Polypeptide cationic micelles mediated knockdown of ZEB1 inhibits metastasis and sensitizes chemotherapeutic drug for cancer therapy.